7 月 7, 2025 | PIF檔案
許多品牌在準備產品上市時,最常見的一個誤解就是:「只要完成產品登錄 ,就算合規 了。」
但實際上,化妝品的合規制度 是雙軌並行 :一方面要完成產品登錄 ,另一方面還要建立產品資訊檔案(PIF) 。本篇文章將帶你了解PIF 與產品登錄的差異 ,帶你一次搞懂誰要做、做什麼 ,讓你可以順利完成檔案文件喔!
產品資訊檔案 PIF 和化妝品產品登錄差別是什麼? 產品資訊檔案 PIF 是什麼? PIF(Product Information File) 是非公開資料,需備妥16 項內容 ,包括製程、檢驗、功效、安全評估與 SA 簽署 。輸入業者、自行製造業者和委託製造業者 都需備齊產品配方、成分、製造過程與經適當評估的安全性資料 。
PIF 可為書面或電子檔,不需主動提交,存於公司以供主管機關查核 。
👉 延伸閱讀:PIF 需要準備哪 16 項資料?一篇圖解給你看
化妝品產品登錄是什麼? 化妝品產品登錄 是根據《化粧品衛生安全管理法第 9 條》進行,廠商必須透過化粧品產品登錄系統 登錄產品名稱、品牌、成分、用途、劑型、製造地等資料。
立即登錄 👉化粧品產品登錄系統系統
誰負責做 PIF?誰負責做化妝品產品登錄? PIF 需交由有 SA 得安全評估員簽核 產品資訊檔案(PIF )必須經由具備資格的安全評估人員(SA, Safety Assessor) 簽署確認。這名 SA 必須具備相關專業背景 ,例如藥學、毒理學、醫學或化妝品相關科系畢業 ,並經過考核認證 才能進行產品評估。
👉 延伸閱讀:PIF 不是誰都能簽!你的化妝品安全資料簽署人(SA)找對了嗎?
化妝品產品登錄通常由販售商於線上進行申請 化妝品產品登錄通常由業者申辦 ,包括品牌商、經銷商,或具有自有品牌販售的代工廠 ,因為化粧品產品登錄系統 需要使用工商憑證 IC 卡登入 ,或是向衛福部致函申請帳號 (需檢附公司、工廠或商業登記證明文件影本 ),才能順利完成線上登錄流程 。
PIF 和化妝品產品登錄重點時程一次掌握 產品資訊檔案 PIF 時程 台灣自2024 年起正式啟動 PIF(產品資訊檔案)制度 ,依《化粧品衛生安全管理法》分三階段推行 ,預計於2026 年 7 月全面上路 。屆時所有一般化粧品(免工廠登記之固態手工香皂除外) 皆須建立 PIF ,否則不得上市 。
化妝品產品登錄時程 從2024 年 7 月起 ,化粧品不分「一般」或「特殊」,每一項產品都要完成登錄 才行,千萬別漏登喔!
登錄與 PIF 是雙軌並行,不可偏廢! 在法規越趨嚴謹的趨勢下,合規不只是為了避免罰則,更是品牌建立信任、穩定經營的基本門檻 。許多品牌誤以為「完成登錄就合規」 ,實際上這只是第一步 ,真正攸關安全審查與法規罰則的,是完整且具簽署的 PIF 檔案 。
選擇與專業團隊「標準認證 」合作,協助你從建檔到簽核一次到位,穩健打造品牌合規力 !
參考資料 衛生福利部食品藥物管理署-化粧品產品資訊檔案(PIF)專區 衛生福利部-113年7月1日起 化粧品不分類 迎接管理新時代
7 月 1, 2025 | 法規新訊
衛福部食品藥物管理署日前公告,自 2025 年 7 月 1 日起 ,化粧品產品資訊檔案(Product Information File, PIF)制度 將正式邁入第二階段 。包括嬰兒用 、唇用 、眼部用化粧品 ,以及非藥用牙膏與漱口水 等產品,業者須在產品上市前完成PIF 建置 ,並經安全簽署人員 確認資料內容,以確保消費者使用安全 。
讓合規變品牌力,標準認證啟動 PIF 一站式整合服務 面對法規上路,美妝產業迎來全新挑戰與轉型契機。過去被視為「合規成本」的PIF ,如今已成為品牌能否順利上市、取得市場信任的必要條件,標準認證 公司近期推出PIF 合規整合服務 ,結合市場趨勢報告 、AI 簽核系統 與媒體行銷資源 ,協助品牌將合規轉化為品牌力,從被動應對轉為積極佈局。
標準認證指出,美妝新品從研發到上市,常面臨三大隱性成本壓力 。首先是法規流程不清,導致品牌必須反覆調整包材設計、配方與標示內容,耗費時間與資源;其次是部門間缺乏橫向整合,研發、法務與行銷資訊難以同步,降低整體效率;最後則是上市時程與法規審核進度未能對齊,影響產品上市時機與聲量發酵。
為此,標準認證 導入AI 智能審核系統 與法規風控預警機制 ,協助品牌快速完成PIF 建置 ,提升整體簽核效率,同時降低人為錯誤與重工風險;另一方面,透過全球美妝市場監測機制 ,每月提供國際趨勢 與國內輿情分析 ,幫助品牌即時掌握市場脈動佈局新品策略。而針對已完成簽核的產品,標準認證 亦整合一線媒體 提供免費曝光 ,讓PIF 不再只是法規責任,更成為新品行銷的起點 ,有效強化品牌信任度 。
PIF 不只是通行證,更是品牌價值的起點 2026 年 7 月起PIF 制度將全面實施 ,標準認證呼籲,對於尚未啟動建置流程的品牌方、製造商、經銷商,應盡早整合資源、展開準備。啟動規劃 ,將合規成本轉為品牌紅利 。」
標準認證執行團隊強調,面對制度落地與市場趨嚴的雙重壓力,提前布局 才能贏得主導權 ,而標準認證所提供的三大整合服務 ,正是協助品牌迎戰PIF 制度浪潮 、穩健走向市場的助力。
參考資料 衛生福利部食品藥物管理署-化粧品產品資訊檔案(PIF)專區 潮健康-化粧品 PIF 第二階段上路!7 月起嬰兒用、牙膏選購更安心
6 月 24, 2025 | 法規新訊
天氣越來越熱, 防曬噴霧 、 保濕噴霧 、 香體噴霧 幾乎成了大家夏天的 隨身好物 。
身為 美妝品牌 的你可能也正在 布局噴霧市場 ,務必要注意:衛福部於 2025 年 6 月 23 日訂定了《 噴霧狀化粧品之使用安全指引 》。
👉 本文整理 新法規 資訊,帶你掌握 產品該怎麼標 、 仿單怎麼寫 ,幫助你 合法又安心上架噴霧型產品 !
什麼是噴霧狀化粧品? 什麼是噴霧狀化粧品? 只要你的產品是 會噴出霧狀 的,不管是 壓一下 還是用 氣罐加壓 噴出來的,都算是 噴霧狀化粧品 。也就是說,不論是 手壓瓶 、 氣罐瓶 ,通通都要遵守 相關安全規範 喔!
你家的產品只要是這些,就是噴霧狀化粧品! ✔️ 防曬噴霧
2025 年噴霧狀化粧品法規規範 加壓噴霧使用與標示規範 衛福部明訂 , 加壓噴霧產品 必須在 外包裝 、 容器 、 標籤 或 仿單 中刊載相關注意事項:
🚫 請勿持續噴灑於同一部位,以免造成皮膚凍傷 🔥 使用時應遠離火源、熱源或電源 🌞 請勿長時間置於陽光直射處或高溫環境,如汽車內 🧯 請勿破壞容器或焚燒 通用型噴霧產品的安全建議(加壓與非加壓皆適用) 品牌 應於 標示中 加註以下 通用安全提醒 :
✅ 使用時與施用部位保持適當距離(建議 15~20 公分) 👁 避免噴入眼睛、口鼻或其他黏膜部位 💨 應在空氣流通處使用,避免直接吸入噴霧 🧒 供兒童使用之化粧品應在成人監護下使用 🚫 產品應放置於兒童伸手無法觸及處 分類 加壓噴霧 非加壓噴霧 保存方式 請勿長時間置於陽光直射處或高溫環境(如汽車內),應置於陰涼乾燥處。 - 容器安全 請勿破壞容器或焚燒。 - 使用方式 1. 請勿持續噴灑於同一部位,以免造成皮膚凍傷。 - 使用時與噴灑部位應保持適當距離。 使用安全 1. 避免噴入眼睛或黏膜等部位。 兒童安全 1. 供兒童使用之化粧品應在成人監護下使用。 成分標示 如添加其他應標示成分,應依規定辦理。
噴霧化粧品也可以同步納入產品資訊檔案(PIF) 自 2026 年 7 月起 , 品牌 在 上架前 必須同步建立 產品資訊檔案(PIF) ,針對 噴霧狀化粧品 ,應依規定將下列資訊納入 PIF 第四大項「產品標籤、仿單、外包裝或容器上」 明確標示。
👉 PIF 是什麼?2026 年強制實施!你的品牌準備好了嗎?
品牌對於噴霧狀化粧品的 4 大行動指南 1. 確認產品劑型 加壓 或 非加壓噴霧 的產品,再來套用對應 法規 。
2. 檢查產品標示 包裝 、 容器 與 仿單 已載明所有必要 警語 ,如 使用距離 、 火源避免 、 高溫警示 、 兒童監護 …等。
3. 修正包裝、容器、仿單內容 噴霧狀化粧品使用安全指引 》調整 使用建議 與 注意事項 ,讓 消費者一目了然 。
4. 建立 PIF 文件 安全指引 與 標示條目 納入 PIF 「第四大項」外包裝、容器、標籤或仿單標示 中,為 2026 稽查提早布局。
掌握《噴霧狀化粧品之使用安全指引》讓產品合規又安心 2025 年《噴霧狀化粧品之使用安全指引》正式上路, 掌握正確標示規範 、 設計清晰易懂的使用說明 ,再結合 完整的法規文件 與 PIF 建置 ,將幫助你的 品牌合法上架 , 建立市場信任感 。
參考資料 衛生福利部食品藥物管理署-噴霧狀化粧品之使用安全指引 衛生福利部食品藥物管理署-藥物食品安全週報
6 月 21, 2025 | PIF檔案
你也在為找 PIF 代辦傷腦筋嗎?面對 2026 年即將全面上路的 PIF 制度 ,不少品牌開始加緊腳步尋求專業協助,但市面上的代辦服務五花八門,報價落差大、品質參差不齊 ,讓人難以下決定。選錯合作對象,不只可能被退件、延遲上市 ,還可能讓你白白浪費時間與成本。
本篇整理出 挑選 PIF 代辦服務的 3 個關鍵要素 ,包含 人員資格、時程控管與整合能力 ,幫你精準選擇 PIF 代辦!
為什麼你需要 PIF 代辦服務? 如果不熟悉法規,自己做容易出錯 雖然衛福部有提供查檢表與範例,但實際執行時,每項資料都牽涉專業法規、格式要求與資料出處的查核 。許多品牌在實際操作時才發現,內容包含產品配方、安全評估、製造流程 …等項目,根本不知道該如何展開整理。
因此,選擇專業的 PIF 代辦,不只能降低錯誤風險,更能節省寶貴的準備時間 。
不是簽完就好,還要懂幫你追蹤與應用 PIF 並非一勞永逸的文件,法規可能更新、原料可能禁用、商品可能改版 ,這都會影響你原本建立的產品資訊檔案,選擇專業代辦服務,能協助你追蹤最新法規變動,確保資料即時調整、不落後、不違規 !
如何挑選最適合的 PIF 代辦服務?這 3 大關鍵必懂! PIF 代辦中的 SA 顧問是否具備實戰經驗? 很多品牌為了節省預算,會選擇價格較低的 個人戶 SA(安全評估人員) ,但你確定對方是經驗豐富的實務專家,還是只是 上完課、拿到證書,卻沒有實際操作經驗的人 ?
根據法規,藥學、醫學、毒理、化學等科系畢業者皆可考取 SA 資格 ,但實務上,這些背景的人未必了解化妝品研發與配方實務;特別是一些學術背景出身的 SA,可能缺乏對原料實際運用、配方穩定性、製程風險 …等的整合經驗,未來在安全評估上也可能存在盲點。
建議在選擇 SA 顧問時,不只看證書,更要了解其是否具備完整的實戰經驗與產業敏感度 ,才能避免日後補件、重審甚至退件的風險。
PIF 代辦的簽核時程安排是否可順利完成? 有些工廠為了提供品牌更完整的服務,會一併協助進行 PIF 認證,但通常是由 廠內具 SA 證照的研發人員負責簽核 ,然而這些研發人員本身已有既定開發任務,難以隨時調整節奏或應對突發進度 。
因此,若你打算與工廠配合完成簽核,務必確認是否能簽訂具體時程的合約 ,避免臨近上架才發現延遲、卡關;或者 選擇能即時調整、同步追蹤進度的團隊,守住產品上市節點 ,會是更穩妥的選擇。
PIF 代辦能不能隨時幫你追蹤法規資訊? 台灣的 PIF 制度主要是參考歐盟的法規,未來也可能 因國際法規調整而更新要求 ,同時台灣法規也會不定期更新條文,例如:原料禁用名單擴增、資料格式改版,甚至新增必備佐證項目,這些都可能影響原有檔案的合規性。
因此,選擇的 PIF 代辦團隊是否具備即時追蹤法規變動、主動通知品牌更新需求的能力 ,將會是合作成功與否的關鍵之一,意思是,PIF 簽核 不是交付完就結束,而是要能陪你長期維護與應對未來檢查需求 ,這才是真正值得信任的專業團隊。
標準認證不只做 PIF,而是你策略性的美妝夥伴 許多 PIF 代辦服務只專注於合規流程,但我們想跟著你一起走得更遠。
我們懂的不只是法規,更懂新品上市的節奏與痛點 我們從開發階段就介入,不只是簽核,而是 整合市場資訊 、PIF 認證 與 媒體曝光 ,讓你 一份預算放大效益,快速建立產品競爭力 。
三大整合服務,幫你贏在起跑點 我們提出的「一包預算三項服務」方案,針對品牌從開發到上市的全流程設計,讓你在有限預算中達到最大效益:
① 全球市場洞察|支援產品開發 每月 透過趨勢數據與熱門成分分析,幫你整合市場資訊 ,掌握消費者需求與競品動態,協助你制定更聚焦的研發策略。
② 法規簽核導入 AI|提升效率與精準度 結合 AI 工具與專業顧問團隊,提高 PIF 審核精準度,並有效縮短簽核時程 ,同時同步追蹤後續法規異動,確保資料即時更新、合規不中斷。
③ 媒體曝光支援|強化聲量與轉換 行銷預算被 PIF 吃掉?這一包預算還包含 免費媒體曝光資源,將合規內容轉化為新聞亮點 ,幫助你建立品牌信任、擴大聲量,搶占消費者第一印象。
傳統代辦 標準認證美妝整合顧問服務 文件處理時間 30-45 天 14-21 天 法規監控 大部分為人工監控 AI+法規風控預警系統 行銷推廣 無 媒體新聞曝光 市場分析 無 全球市場趨勢報告
PIF 代辦服務比較表
PIF 代辦就選標準認證! 在產品競爭激烈、法規日趨複雜的今天,PIF 不再只是法規門檻,更是品牌策略與上市節奏的關鍵一環 。
選擇懂品牌、懂行銷、懂法規的顧問團隊,才能從合規邁向曝光,實現產品價值最大化 ,立即加入我們 LINE,由專人為你服務,啟動你的品牌進化之路!
參考資料 衛生福利部食品藥物管理署-化粧品產品資訊檔案(PIF)專區 衛生福利部食品藥物管理署-化妝品產品資訊檔案管理辦法
6 月 21, 2025 | PIF檔案
你知道嗎?一份 完整且合規的 PIF(產品資訊檔案) ,竟然包含多達 16 項資料欄位 !很多品牌常常卡關在: 不知道要準備哪些內容 、文件格式錯誤 ,或是 資料不一致 等問題。
本篇將以 圖解懶人包 的方式,一次整理出這 16 項必備資料,幫助你掌握 分類邏輯 與 資料來源建議 ,從 法規合規 到 製程提效 ,讓準備流程更 省時又省力 !
🧩 第一大類:產品敘述(共 8 項) 產品敘述類別 是整份 PIF 的 基礎核心 ,內容涵蓋 產品名稱、用途、製造廠商資訊、成分與標示 等,所有細節都必須與 實際產品包裝 及登錄系統 資料 完全一致 。
以下是每項細部內容的說明與資料來源建議:衛福部「化粧品產品資訊檔案查檢表」 來輔助檢查喔!
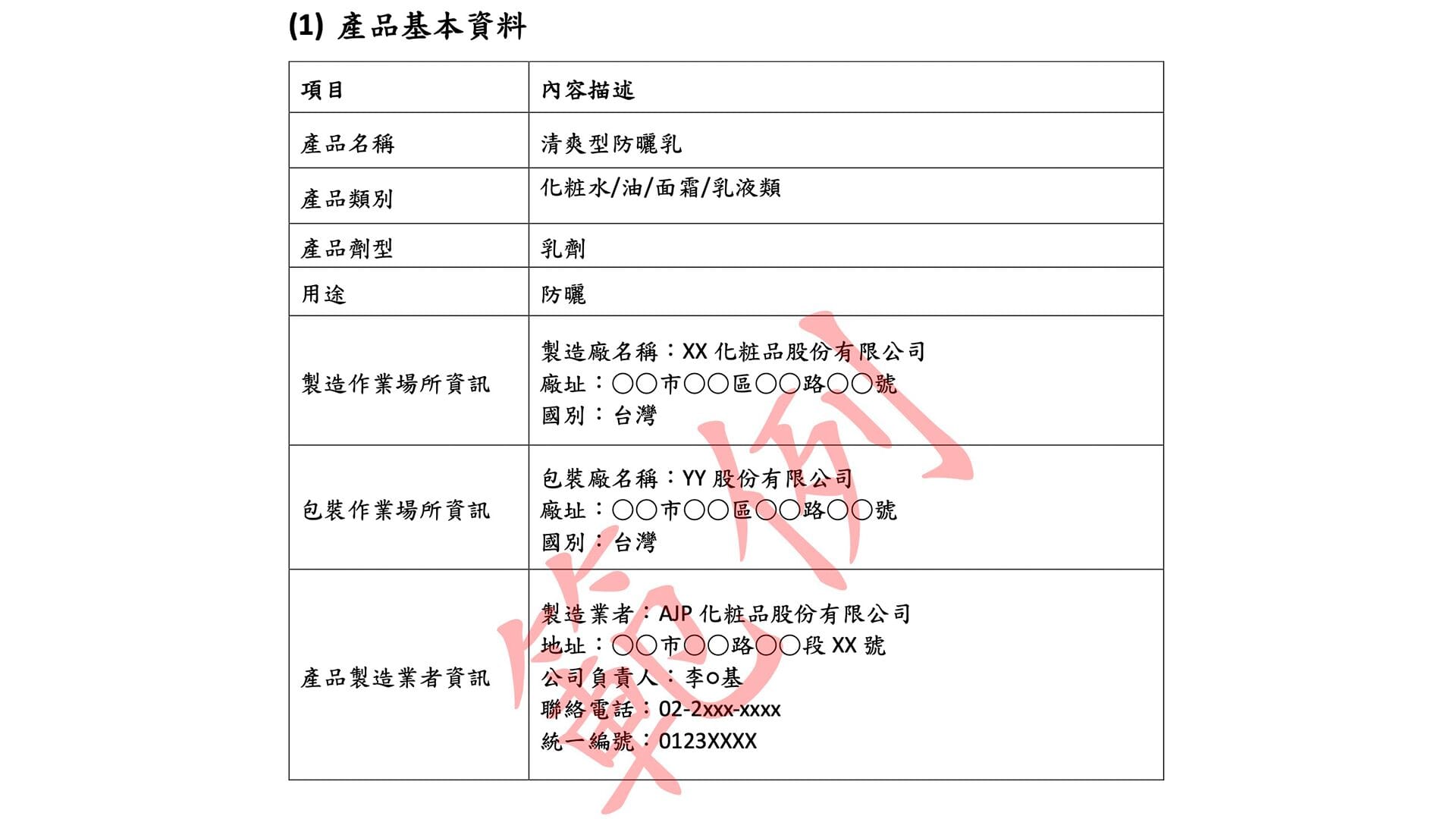
1. 產品基本資料 產品名稱 :需載明實際產品名稱,與包裝標示一致。產品類別與劑型 :說明產品屬於哪一類化粧品,並標明其劑型形式(如乳霜、液體、凝膠…等)。用途說明 :明確陳述產品的使用目的,並確保宣稱用途 符合化粧品定義 。製造廠資訊 :列出製造廠 名稱與地址 …等基本資訊。製造或輸入業者資訊 :提供業者的 名稱、地址與聯絡電話 …等完整資料。💡小提醒:製造作業場所資訊 、包裝作業場所資訊 、產品製造業者資訊 如果各自不同,記得都要一一列出來 喔!
範例 資料來源建議:由品牌方/業者整理
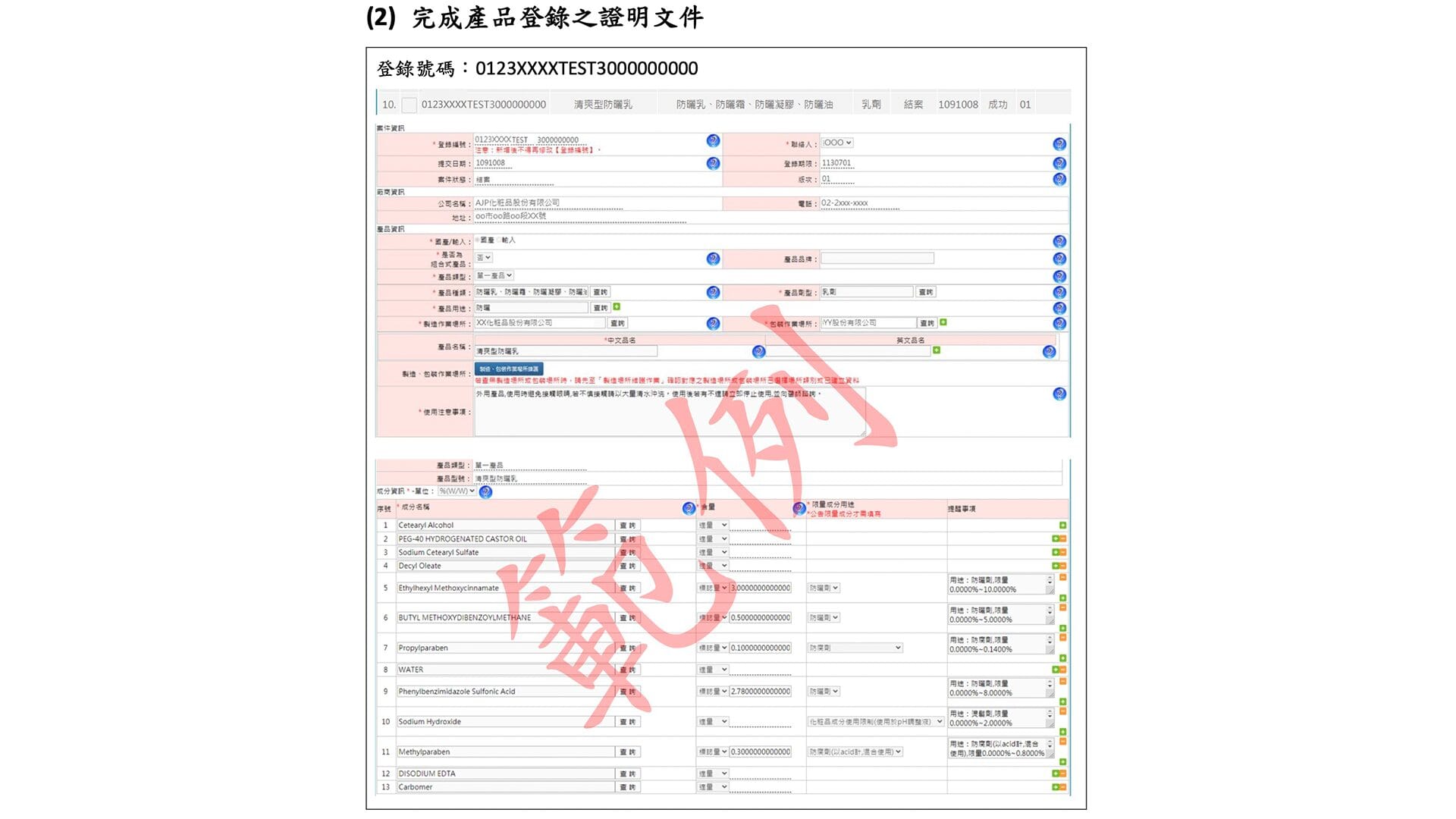
2. 產品登錄證明文件 完成 產品登錄 後,需確認 系統填寫資料 與 PIF 留存內容一致 。
💡小提醒:基本資料 應與 化粧品登錄系統 填寫內容 完全一致 !
👉 不知道怎麼申請化粧品產品登錄? 來看看詳細指南
範例 資料來源建議:由品牌方/業者提供
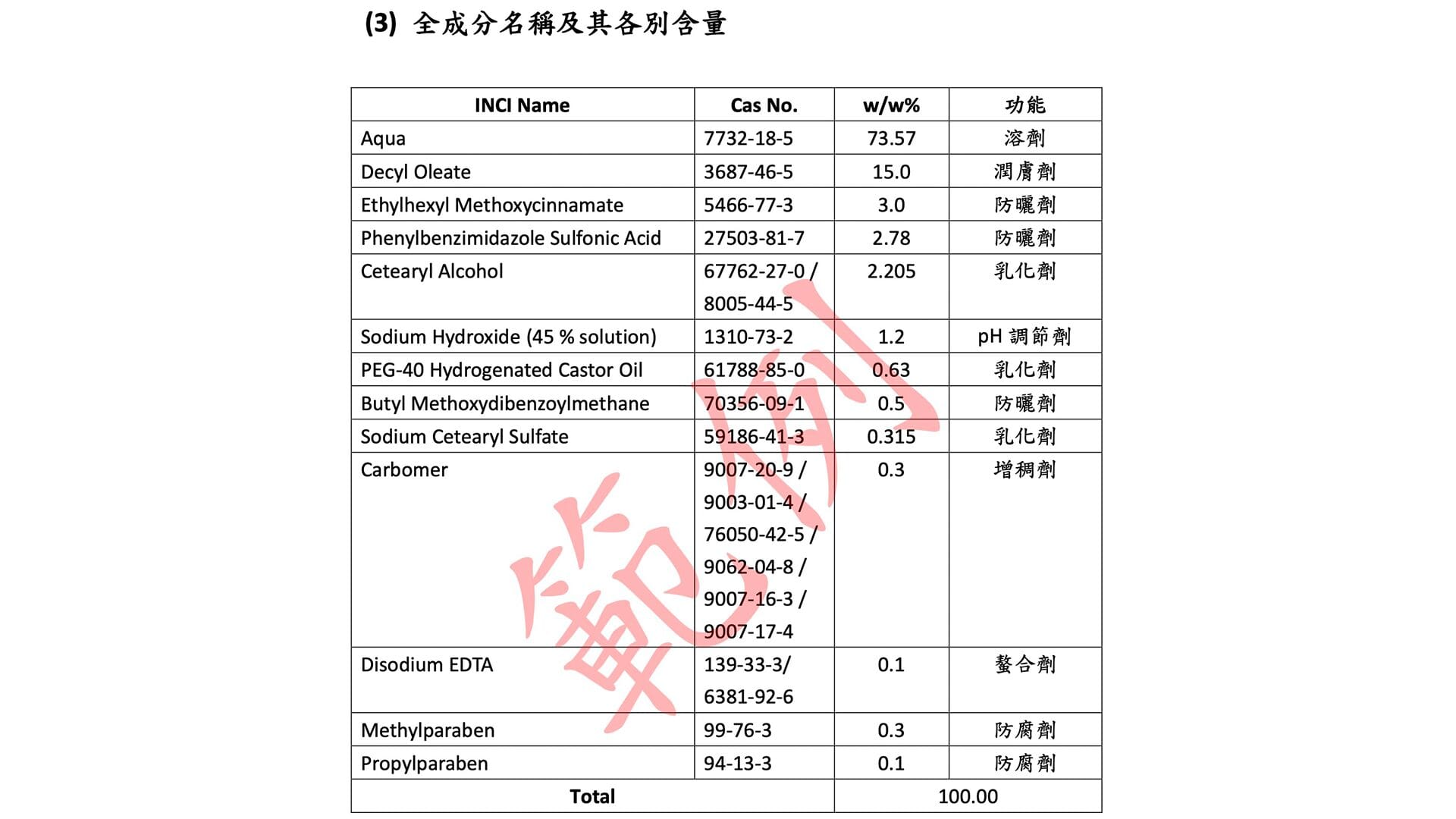
3. 全成分名稱及其各別含量 需 完整列出所有成分 ,包含:限用成分、防腐劑、著色劑 及 其他成分 的 名稱與含量 ,並依據 《化粧品原料基準》 、 《中華藥典》 或 INCI 國際命名 規範進行標示。
📌標示規則:
色素標示方式 :可參考 美國 FDA 的 Color Index (CI) 或 EC Directive Annex IV 命名法 。香精及香料 :可使用「 香精、香料、Flavor、Fragrance、Parfum、Perfume、Aroma 」等通用名稱,同時需提供供應商名稱 。法規遵循 :所有成分使用必須符合《化粧品衛生安全管理法》第6條 及相關規定。含量表示方式 :請以 重量百分比(W/W%) 或 容量百分比(W/V%) 標示。💡 小提醒:提供 詳細成分配比 ,記得檢查 總合是否為 100% 喔!
範例 資料來源建議:請代工廠/製造商提供
4. 產品標籤、仿單、外包裝或容器 外包裝或容器上的刊載事項,必須依據《 化粧品衛生安全管理法》第7條 與 「化粧品外包裝、容器、標籤或仿單之標示規定」 辦理,確保資訊正確且完整。
💡小提醒:若為 進口產品 ,務必加註 「原產地(國)」欄位及內容 !
👉 詳細資訊請見:衛福部食藥署《化粧品外包裝、容器、標籤或仿單之標示規定》
範例 資料來源建議:由品牌方/業者提供
5. 製造場所合規證明 需提供符合化粧品優良製造準則(GMP) 的 證明文件或聲明書 ,以確認製造場所具備合法與安全生產條件。
💡 小提醒:記得檢查證書是否過期 ,確保文件效期在有效範圍內!
範例 資料來源建議:請代工廠/製造商提供
6. 製造方法與流程 可採用 文字說明 或 流程圖示 ,說明產品的整體 製造過程 ,也可提供 標準作業程序(SOP) 、生產紀錄 與 品質管制文件 等作為補充資料。
💡 小提醒:流程一定要標示到「成品階段」 ,才算完整喔!
範例 資料來源建議:請代工廠/製造商提供
7.使用方法與適用對象 須清楚說明產品的 使用方式 、使用部位 、建議用量 、使用頻率 ,以及 適用族群 等相關資訊。
💡 小提醒:可善用 包裝上的文字或圖示 來輔助說明,讓使用說明更清楚易懂!
範例 資料來源建議:由品牌方/業者提供
8. 不良反應資料(如沒有則不需提供) 應妥善保存產品使用後的 不良反應紀錄 ;若發生 嚴重不良反應 ,需 主動通報主管機關 。
📌 資料來源建議:
若有相關紀錄,應由 品牌方或業者提供 。 若無不良反應資料,則由 SA 安全評估人員 出具 「無不良反應資料」說明 以資佐證。 🧪 第二大類:品質資料(共 5 項) 9. 產品與成分之物理與化學特性 需說明 產品 及 各別成分 的 基本物理與化學特性 ,包含以下兩大內容:
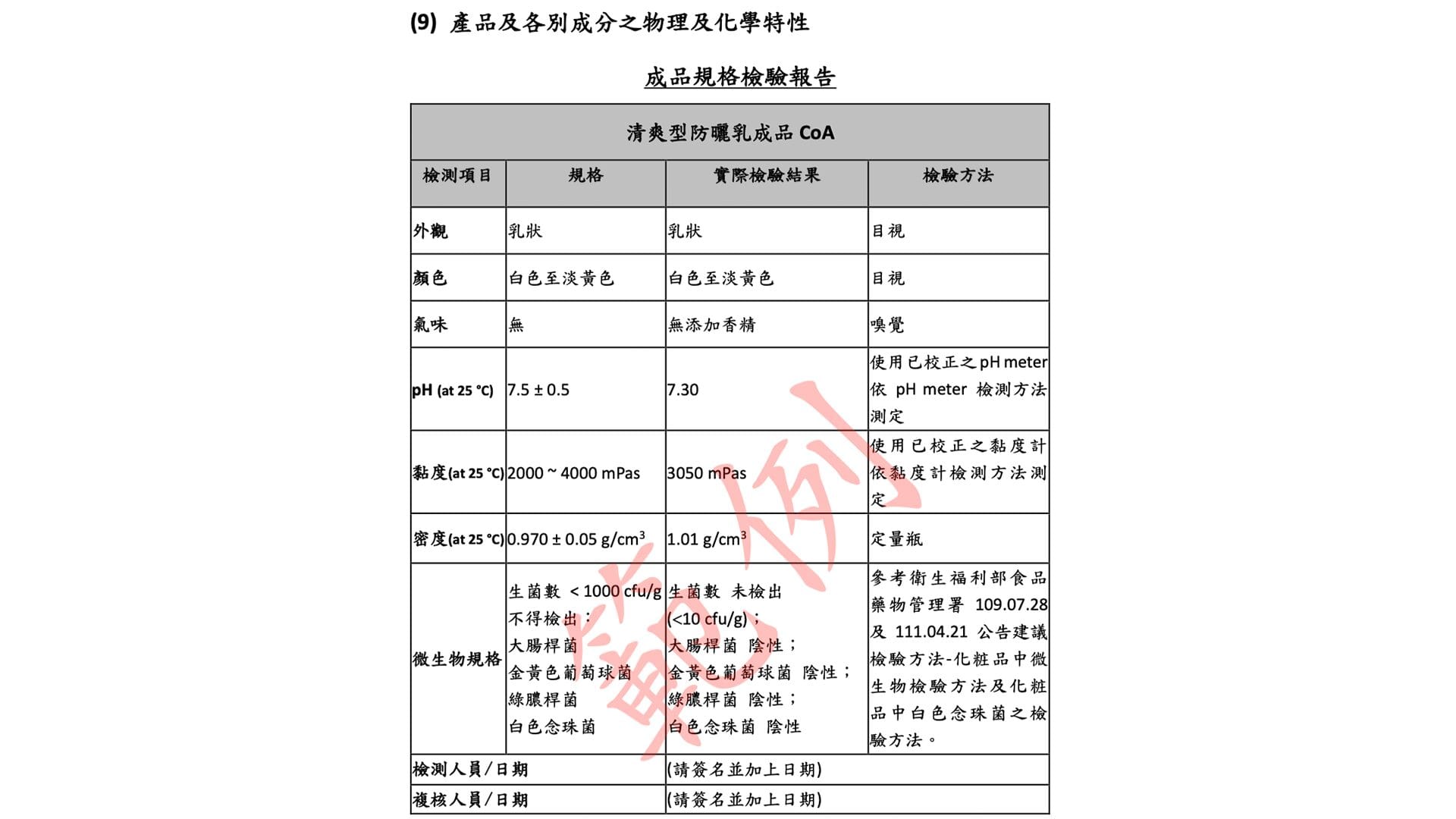
整體產品的品質規格 :如外觀、氣味、pH 值、黏度、穩定性…等。各項成分的品質規格 :例如 pH 值、純度、規格…等相關指標。👉 物理與化學特性資料哪裡來?這些資料裡都會有 MSDS、COA、TDS
範例 資料來源建議:請代工廠/製造商提供
10.成分毒理資料 需提供 每一項成分 的 毒理學資料 或 安全性相關數據 ,作為 產品風險評估 的重要依據。
這些資料通常由 毒理資料庫 、原料供應商技術文件 或 文獻研究報告 取得,作為 SA 進行安全性評估的重要判斷基礎。
範例 資料來源建議:由標準認證機構 / 合格 SA 顧問提供
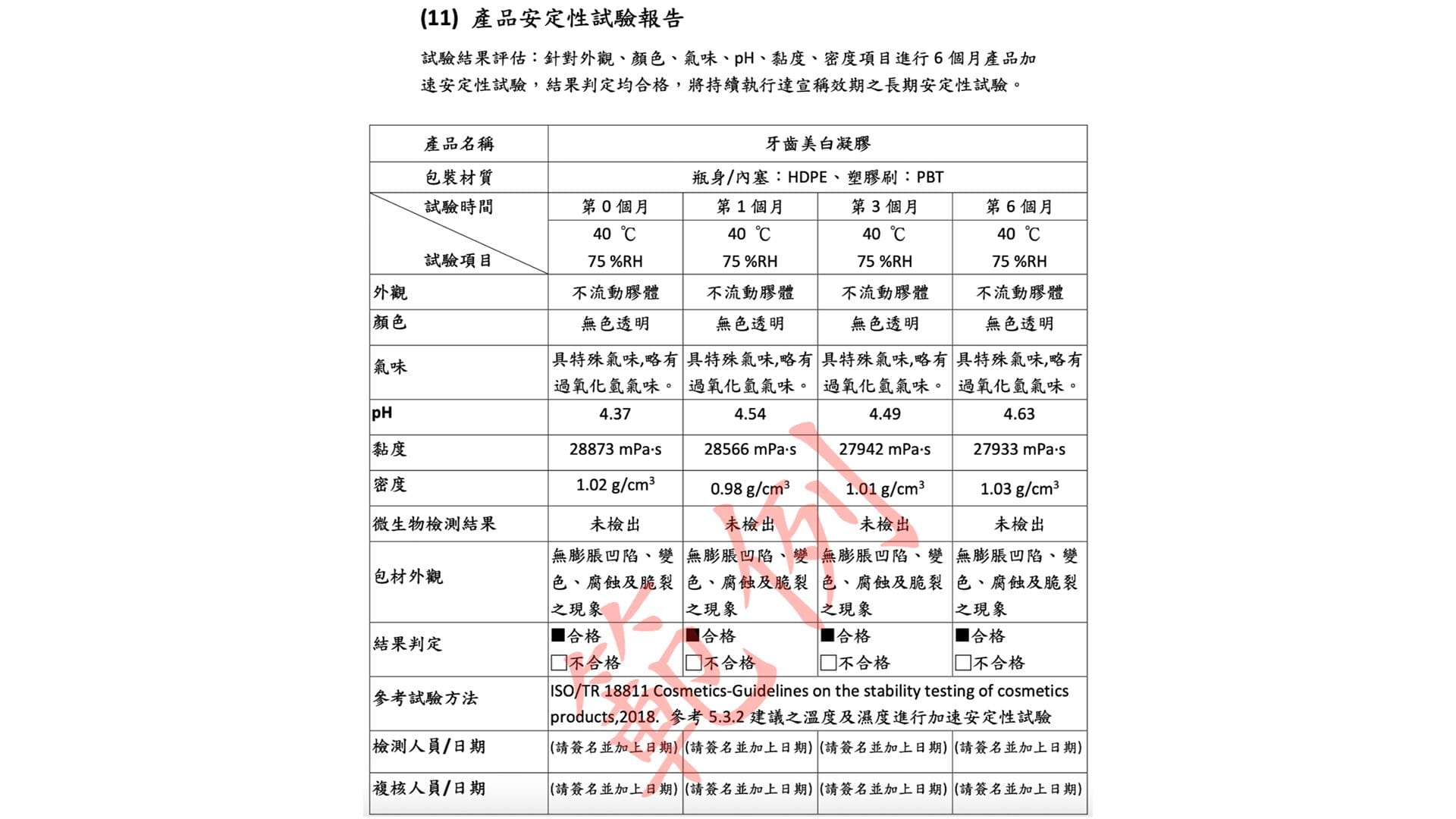
11. 產品安定性試驗報告 需提供產品於 正常儲存條件 下進行的 安定性試驗數據 ,作為產品 品質穩定 的依據與證明。
試驗內容通常包括:外觀變化、氣味、pH 值、黏度 …等指標是否在預期範圍內,確保產品在保存期限內仍具使用安全性與功能性。
範例 資料來源建議:由代工廠/製造商(如有檢測服務)/檢驗商檢測
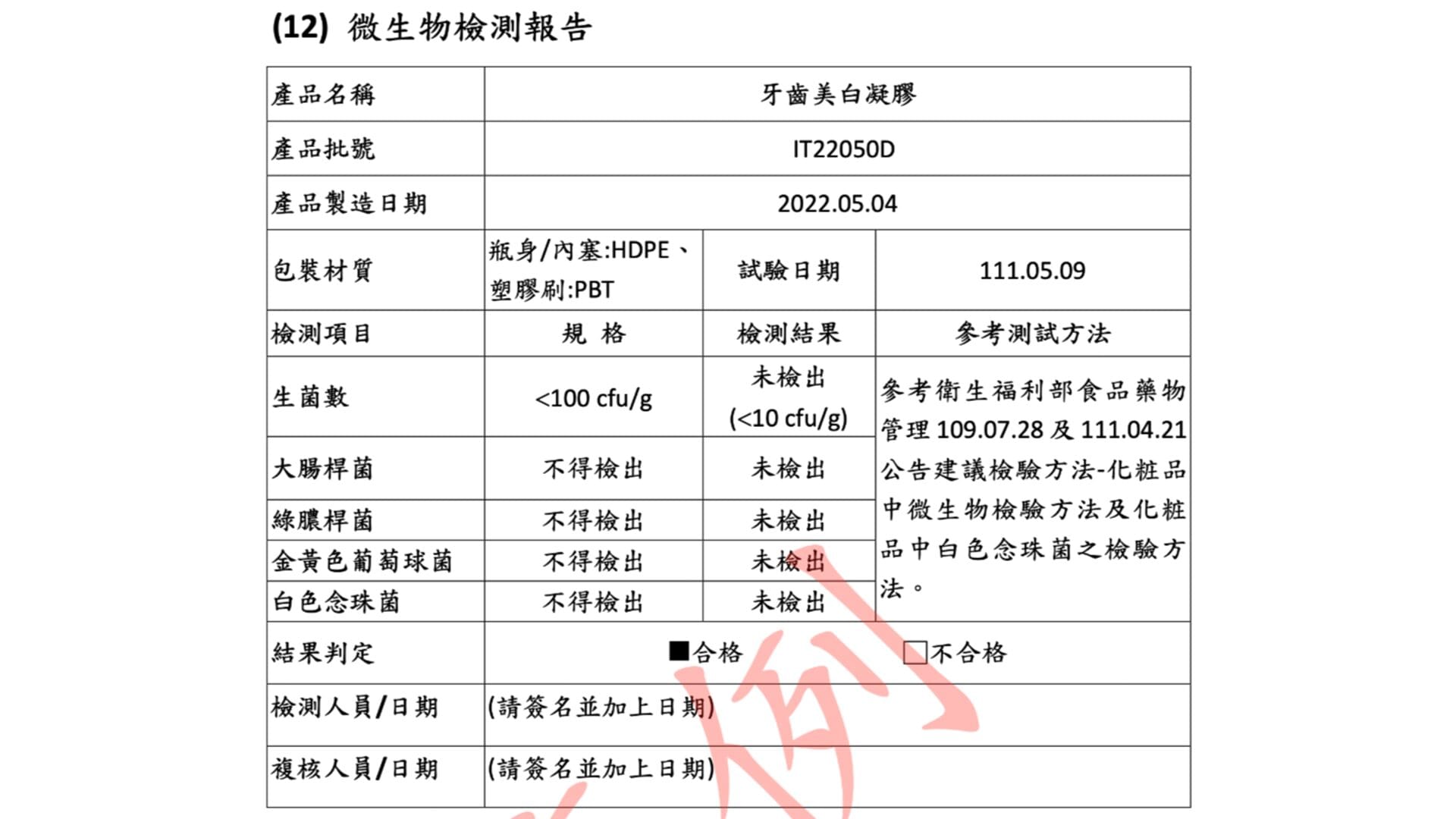
12.微生物檢測報告 需確認產品符合 微生物衛生安全標準 ,確保 不含超量致病菌 或 污染風險 ,報告內容應包含以下三大部分:
微生物控制標準與規格 :說明產品設定的 微生物管理目標值 與 允收範圍 。檢驗所採用的標準方法 :須明確載明所使用的 國際(如 ISO) 或 國內(如衛福部公告標準) 的檢測依據。實際檢驗結果 :完整呈現 檢驗數據 ,並確認其結果符合 《化粧品微生物容許量基準表》 規定。👉 因微生物污染被下架!你的產品過得了微生物檢測嗎?檢測標準一次看懂
範例 資料來源建議:由代工廠/製造商(如有檢測服務)/檢驗商檢測
13.防腐效能試驗報告 若產品 添加防腐劑 ,應提供 防腐效能試驗的檢驗方法 與 完整試驗報告 ,以證明產品在使用期間可有效抑制微生物滋生。
若屬於 低風險產品 (例如:單次使用、小容量包裝、或不開封接觸的設計),可依規定 免除試驗 ,但仍需提出 「無需防腐效能試驗」的證明資料 以供佐證。
👉 微生物檢測只是基本!產品開封後要能安心使用,化粧品防腐效能試驗才是關鍵
範例 資料來源建議:由代工廠/製造商(如有檢測服務)/檢驗商檢測
🧾 第三大類:功能性佐證資料(共 1 項) 14.功能評估佐證資料 若產品宣稱具 特定功能 (如 抗痘、美白、保濕 …等),必須提供相應的 功效佐證資料 。
這些資料通常須透過 第三方機構測試 取得,並應包含 測試方法、實驗設計、數據結果與結論 ,以具體支持所宣稱之效果,符合 化粧品標示不得誇大不實 的法規要求。
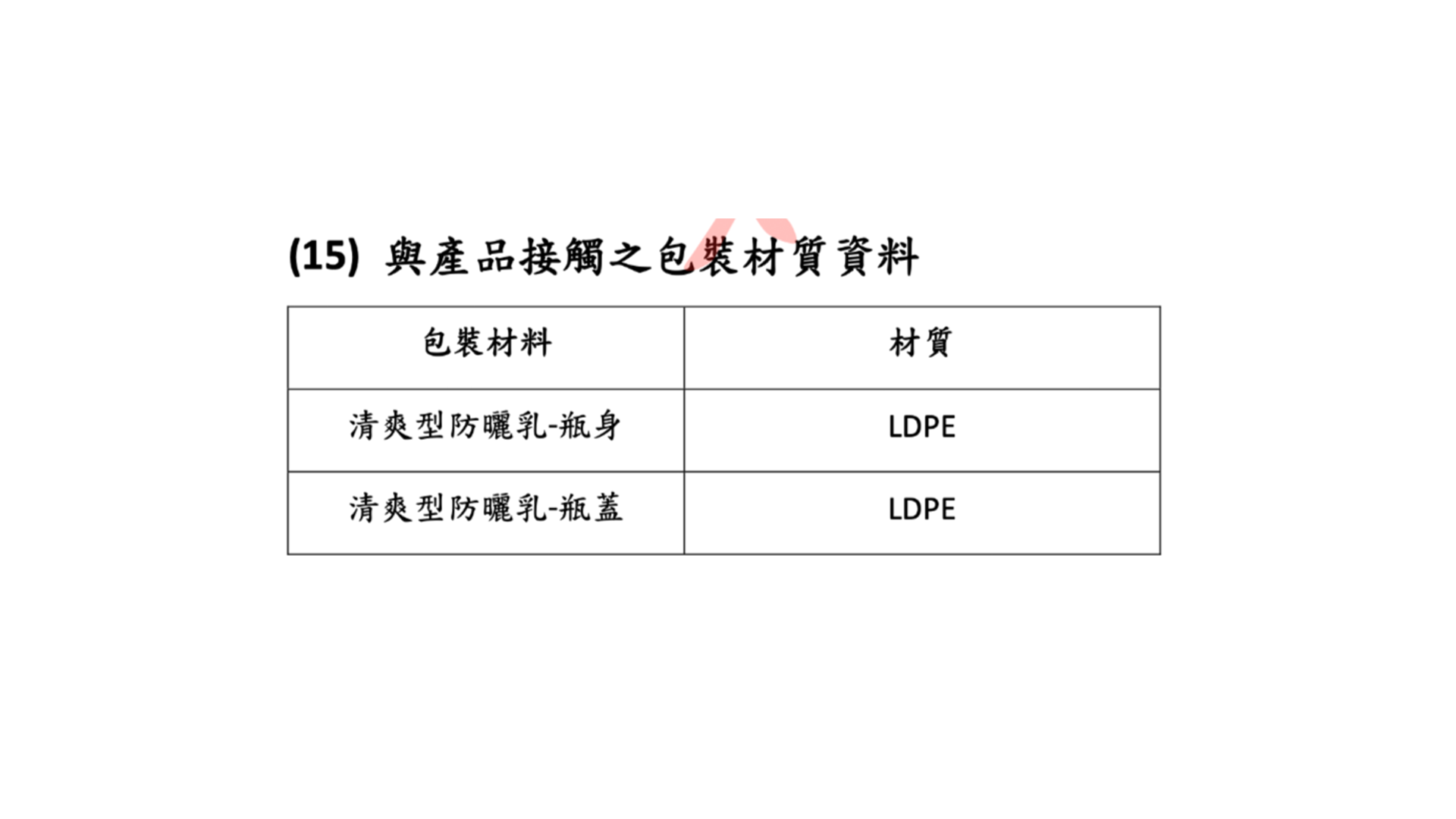
🔐 第四大類:安全評估資料(共 2 項) 15.與產品接觸之包裝材質資料 須提供 與產品直接接觸的內包裝材質 資訊,包括其 材質規格 與 容量大小 …等基本資料。
範例 資料來源建議:由包材商/代工廠/製造商提供資料
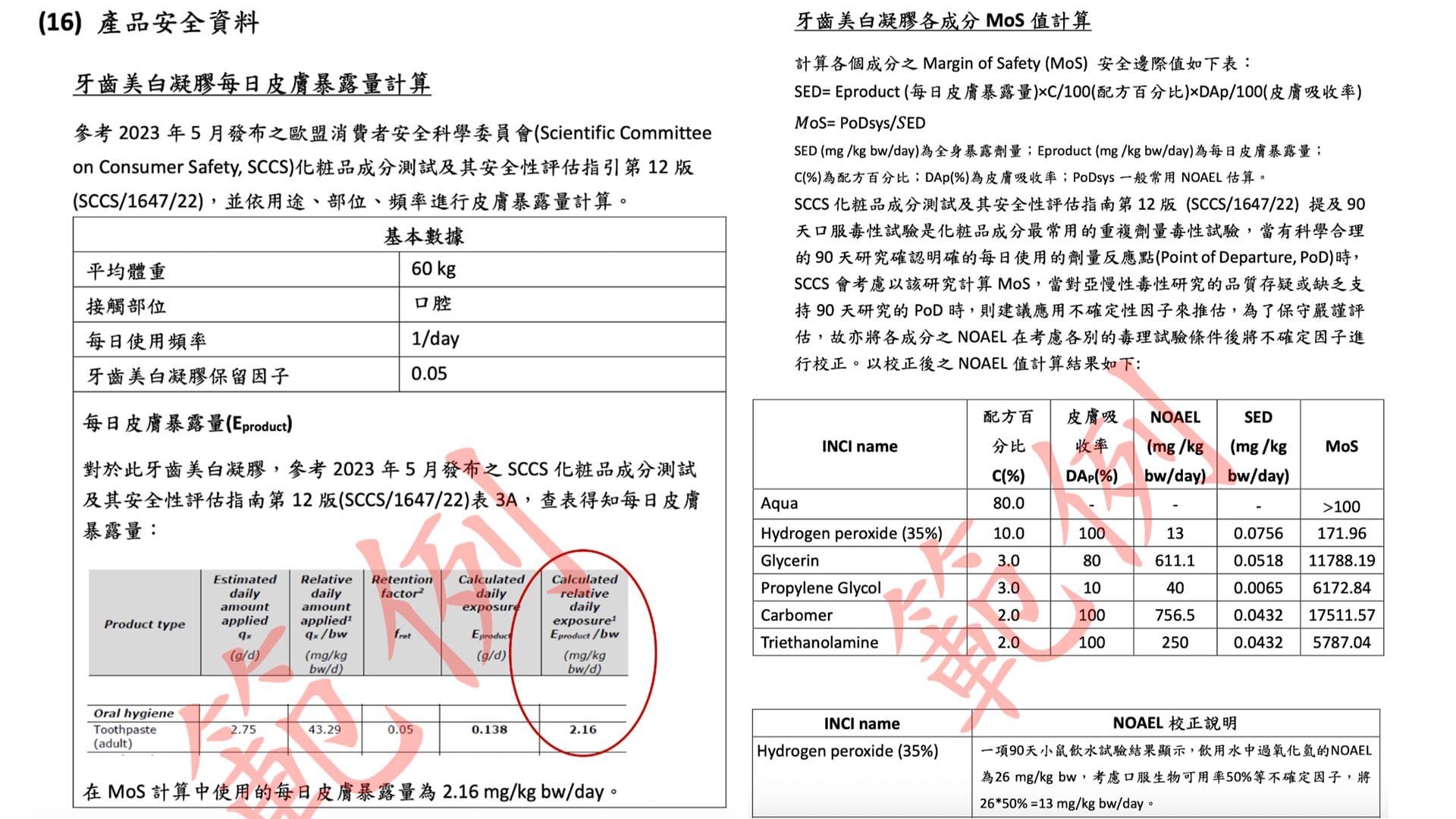
16.產品安全資料 本項為整份 PIF 的 最終核心文件 ,需由 具備資格的安全資料簽署人員(SA) 進行評估與簽署,並提供以下資料:
安全性評估結論與建議 整體產品使用風險 ,並包含 具名簽署 與 簽署日期 。簽署人員資格佐證資料 化粧品安全性評估訓練合格證明 、每年複訓證明 …等。💡 小提醒:沒有合法 SA 的評估與簽名,整份 PIF 將被視為 不具效力 ,產品亦無法合規上市。
範例 資料來源建議:由標準認證機構 / 合格 SA 顧問提供
💬 TOP 8 準備 PIF 檔常見疑問|FAQ 懶人包 Q1.交給代工做的產品,PIF 還要品牌負責嗎? A1. 當然要! 根據法規,PIF 是由 「產品責任人」 負責建立,而這個角色通常就是 品牌方 。就算找的是大型 OEM/ODM 代工廠,也不代表對方會主動幫你準備好所有文件唷~
Q2.複方香精要提供每一項成分嗎? A2. 是的! 香精的 「成分組成表」 是法規查核重點,不能只寫「香精」 就想帶過,這部分通常可以請 香料供應商、原料商或代工廠 協助提供。
Q3.只是換個香味、顏色、包裝,也需要重新做一份新的 PIF 嗎? A3. 通常需要! 只要在 配方、用途、標示或包裝 上有差異,原則上就視為 不同品項 ,各自建立 PIF;但如果只是 同一配方、同一劑型 ,單純換容量(例如 30ml / 100ml),可請審核單位評估是否可共用。
Q4.在沙龍或美容師用的產品,也要照法規標示? A4. 要的! 不管是否屬於 「專業用途」 ,只要在台灣 有販售或提供使用 ,都算是 市售化粧品 ,就必須符合一般標示規定。
Q5.PIF 一定要用紙本保存嗎?電子檔可以嗎? A5. 可以! 無論 紙本或電子檔 都可以,只要在 主管機關查核時能完整提供 就沒問題。
Q6|製造流程是商業機密,PIF 會不會被公開? A6. 不會。 PIF 是 內部備查文件 ,不會主動公開 ,只有主管機關依法調閱才會查看。若委託代工,建議在 合約中加入保密條款 ,保護雙方權益。
Q7.我只有一款產品,也要做 PIF? A7. 是的! PIF 是 產品層級的文件 ,無論你只有一項商品,或是百款上架,每一款都必須建立 PIF ;剛起步的品牌更要小心,建議找 專業法規顧問或有經驗的代工廠 協助,能幫你少走很多冤枉路(像 標準認證團隊 就很熟門熟路!)
Q8.原始資料是英文,可以整份 PIF 都用英文嗎? A8. 雖然原始資料(像 SDS、成分報告 )多為英文,但整份 PIF 還是建議以中文為主 ,這樣才方便主管機關查核。
想要不費力完成 PIF 審核?推薦選擇標準認證 從產品命名、成分準備、製造流程,到包裝標示與法規佐證,每一環都環環相扣,牽動的不只是通過查核,更是品牌在市場上的信任力。選擇標準認證 ,讓有經驗的專業團隊陪你一步步完成,從資料準備、格式建議,到 SA 安全評估與合規簽署,全程協助、一次到位讓標準認證,成為你邁向市場、連接通路與跨境的穩定後盾。
參考資料 衛生福利部食品藥物管理署-化粧品產品資訊檔案(PIF)專區 衛生福利部食品藥物管理署-化粧品產品登錄平台系統 全國法規資料庫-化粧品衛生安全管理法 衛生福利部食品藥物管理署-化粧品微生物容許量基準表 衛福部食藥署-化粧品外包裝、容器、標籤或仿單之標示規定 衛生福利部食品藥物管理署-化妝品產品資訊檔案管理辦法







.jpg)



.jpg)




.jpg)



.jpg)
.jpg)